2022年青海高考理综真题及答案
注意事项:
1.答卷前,考生务必将自己的姓名、准考证号填写在答题卡上。
2.回答选择题时,选出每小题答案后,用铅笔把答题卡上对应题目的答案标号涂黑。如需改动,用橡皮擦干净后,再选涂其他答案标号。回答非选择题时,将答案写在答题卡上,写在本试卷上无效。
3.考试结束后,将本试卷和答题卡一并交回。
可能用到的相对原子质量:H 1 B 11 C 12 N 14 O 16 Na 23 S 32 Cl 35.5
一、选择题:本题共13小题,每小题6分,共78分。在每小题给出的四个选项中,只有一项是符合题目要求的。
1. 有丝分裂和减数分裂是哺乳动物细胞分裂的两种形式。某动物的基因型是Aa,若该动物的某细胞在四分体时期一条染色单体上的A和另一条染色单体上的a发生了互换,则通常情况下姐妹染色单体分离导致等位基因A和a进入不同细胞的时期是( )
A. 有丝分裂的后期 B. 有丝分裂的末期
C. 减数第一次分裂 D. 减数第二次分裂
【答案】D
【解析】
【分析】减数分裂过程包括减数第一次分裂和减数第二次分裂;主要特点是减数第一次分裂前期同源染色体联会,可能发生同源染色体非姐妹单体之间的交叉互换,后期同源染色体分开,同时非同源染色体自由组合,实现基因的重组,减数第二次分裂则为姐妹染色单体的分离。
【详解】AB、有丝分裂过程中不会发生同源染色体联会形成四分体![]() 过程,这样就不会发生姐妹染色单体分离导致等位基因A和a进入不同细胞的现象,A、B错误;
过程,这样就不会发生姐妹染色单体分离导致等位基因A和a进入不同细胞的现象,A、B错误;
C、D、根据题意,某动物基因型是Aa,经过间期复制,初级性母细胞中有AAaa四个基因,该动物的某细胞在四分体时期发生交叉互换,涉及A和a的交换,交换后两条同源染色的姐妹染色单体上均分别具有A和a基因,减数第一次分裂时,同源染色体分开,两组Aa彼此分开进入次级性母细胞,但不会发生姐妹染色单体分离导致等位基因A和a的现象,而在减数第二次分裂时,姐妹染色单体分离,其上的A和a分开进入两个子细胞,C错误,D正确。
故选D。
2. 某同学将一株生长正常的小麦置于密闭容器中,在适宜且恒定的温度和光照条件下培养,发现容器内CO2含量初期逐渐降低,之后保持相对稳定。关于这一实验现象,下列解释合理的是( )
A. 初期光合速率逐渐升高,之后光合速率等于呼吸速率
B. 初期光合速率和呼吸速率均降低,之后呼吸速率保持稳定
C. 初期呼吸速率大于光合速率,之后呼吸速率等于光合速率
D. 初期光合速率大于呼吸速率,之后光合速率等于呼吸速率
【答案】D
【解析】
【分析】光合作用会吸收密闭容器中的CO2,而呼吸作用会释放CO2,在温度和光照均适宜且恒定的情况下,两者速率主要受容器中CO2和O2的变化影响。
【详解】A、初期容器内CO2浓度较大,光合作用强于呼吸作用,植物吸收CO2释放O2,使密闭容器内的CO2浓度下降O2浓度上升,A错误;
B、根据分析由于密闭容器内的CO2浓度下降,O2浓度上升,从而使植物光合速率逐渐降低,呼吸作用逐渐升高,,直至两者平衡趋于稳定,B错误;
CD、初期光合速率大于呼吸速率,之后光合速率等于呼吸速率,C错误,D正确。
故选D![]()
3. 运动神经元与骨骼肌之间的兴奋传递过度会引起肌肉痉挛,严重时会危及生命。下列治疗方法中合理的是( )
A. 通过药物加快神经递质经突触前膜释放到突触间隙中
B. 通过药物阻止神经递质与突触后膜上特异性受体结合
C. 通过药物抑制突触间隙中可降解神经递质的酶的活性
D. 通过药物增加突触后膜上神经递质特异性受体的数量
【答案】B
【解析】
【分析】兴奋在两个神经元之间传递是通过突触进行的,突触由突触前膜、突触间隙和突触后膜三部分组成,神经递质只存在于突触前膜的突触小泡中,只能由突触前膜释放,进入突触间隙,作用于突触后膜上的特异性受体,引起下一个神经元兴奋或抑制。
【详解】A、如果通过药物加快神经递质经突触前膜释放到突触间隙中,突触间隙中神经递质浓度增加,与突触后膜上特异性受体结合增多,会导致兴奋过度传递引起肌肉痉挛,达不到治疗目的,A不符合题意;
B、如果通过药物阻止神经递质与突触后膜上特异性受体结合,兴奋传递减弱,会缓解兴奋过度传递引起的肌肉痉挛,可达到治疗目的,B符合题意;
C、如果通过药物抑制突触间隙中可降解神经递质的酶的活性,突触间隙中的神经递质不能有效降解,导致神经递质与突触后膜上的特异性受体持续结合,导致兴奋传递过度引起肌肉痉挛,达不到治疗目的,C不符合题意;
D、如果通过药物增加突触后膜上神经递质特异性受体的数量,突触间隙的神经递质与特异性受体结合增多,会导致兴奋传递过度引起肌肉痉挛,达不到治疗目的,D不符合题意。
故选B。
4. 某种酶P由RNA和蛋白质组成,可催化底物转化为相应的产物。为探究该酶不同组分催化反应所需的条件。某同学进行了下列5组实验(表中“+”表示有,“-”表示无)。
实验组 | ① | ② | ③ | ④ | ⑤ |
底物 | + | + | + | + | + |
RNA组分 | + | + | - | + | - |
蛋白质组分 | + | - | + | - | + |
低浓度Mg2+ | + | + | + | - | - |
高浓度Mg2+ | - | - | - | + | + |
产物 | + | - | - | + | - |
根据实验结果可以得出![]() 结论是( )
结论是( )
A. 酶P必须在高浓度Mg2+条件下才具有催化活性
B. 蛋白质组分的催化活性随Mg2+浓度升高而升高
C. 在高浓度Mg2+条件下RNA组分具有催化活性
D. 在高浓度Mg2+条件下蛋白质组分具有催化活性
【答案】C
【解析】
【分析】分析:由表格数据可知,该实验的自变量是酶的组分、Mg2+的浓度,因变量是有没有产物生成,底物为无关变量。第①组为正常组作为空白对照,其余组均为实验组。
【详解】A、第①组中,酶P在低浓度Mg2+条件,有产物生成,说明酶P在该条件下具有催化活性,A错误;
BD、 第③组和第⑤组对照,无关变量是底物和蛋白质组分,自变量是Mg2+浓度,无论是高浓度Mg2+条件下还是低浓度Mg2+条件下,两组均没有产物生成,说明蛋白质组分无催化活性,BD错误;
C、第②组和第④组对照,无关变量是底物和RNA组分,自变量是Mg2+浓度,第④组在高浓度Mg2+条件下有产物生成,第②组在低浓度Mg2+条件下,没有产物生成,说明在高浓度Mg2+条件下RNA组分具有催化活性,C正确。
故选C。
5. 分层现象是群落研究的重要内容。下列关于森林群落分层现象的叙述,正确的是( )
① 森林群落的分层现象提高了生物对环境资源的利用能力
② 森林植物从上到下可分为不同层次,最上层为灌木层
③ 垂直方向上森林中植物分层现象与对光的利用有关
④ 森林群落中动物的分层现象与食物有关
⑤ 森林群落中植物的分层现象是自然选择的结果
⑥ 群落中植物垂直分层现象的形成是由动物种类决定的
A. ①③④⑤ B. ②④⑤⑥
C. ①②③⑥ D. ③④⑤⑥
【答案】A
【解析】
【分析】群落的垂直结构指群落在垂直方面的配置状态,其最显著的特征是分层现象,即在垂直方向上分成许多层次的现象。影响植物群落垂直分层的主要因素是光照,影响动物群落垂直分层的主要因素为食物和栖息空间。
【详解】①森林群落的分层现象在占地面积相同情况下提供了更多空间,提高了生物对阳光等环境资源的利用能力,①正确;
②森林植物从上到下可分为不同层次,最上层为乔木层,②错误;
③影响植物群落垂直分层的主要因素是光照,垂直方向上森林中植物分层现象与对光的利用有关,③正确;
④森林群落中动物的分层现象与食物和栖息空间有关,④正确;
⑤群落垂直结构的分层现象、群落的水平结构等都是自然选择的结果,⑤正确;
⑥群落中植物垂直分层现象的形成主要是由光照决定的,⑥错误。
A正确,BCD错误。
故选A。
6. 依据鸡的某些遗传性状可以在早期区分雌雄,提高养鸡场的经济效益。已知鸡的羽毛性状芦花和非芦花受1对等位基因控制。芦花鸡和非芦花鸡进行杂交,正交子代中芦花鸡和非芦花鸡数目相同,反交子代均为芦花鸡。下列分析及推断错误的是( )
A. 正交亲本中雌鸡为芦花鸡,雄鸡为非芦花鸡
B. 正交子代和反交子代中的芦花雄鸡均为杂合体
C. 反交子代芦花鸡相互交配,所产雌鸡均为芦花鸡
D. 仅根据羽毛性状芦花和非芦花即可区分正交子代性别
【答案】C
【解析】
【分析】根据题意可知,正交子代中芦花鸡和非芦花鸡数目相同,反交子代均为芦花鸡,说明控制鸡羽毛性状芦花和非芦花的基因位于Z染色体上,且芦花为显性。
【详解】A、根据题意可知,正交为ZaZa(非芦花雄鸡)×ZAW(芦花雌鸡),子代为ZAZa、ZaW,且芦花鸡和非芦花鸡数目相同,反交为ZAZA×ZaW,子代为ZAZa、ZAW,且全为芦花鸡,A正确;
B、正交子代中芦花雄鸡为ZAZa(杂合子),反交子代中芦花雄鸡为ZAZa(杂合子),B正确;
C、反交子代芦花鸡相互交配,即ZAZa×ZAW,所产雌鸡ZAW、ZaW(非芦花),C错误;
D、正交子代为ZAZa(芦花雄鸡)、ZaW(非芦花雌鸡),D正确。
故选C。
7. 生活中处处有化学,下列叙述正确的是
A. HB铅笔芯的成分为二氧化铅 B. 碳酸氢钠可做食品膨松剂
C. 青铜和黄铜是不同结构的单质铜 D. 焰火中红色来源于钠盐灼烧
【答案】B
【解析】
【详解】A.铅笔芯的主要成分为石墨,不含二氧化铅,A错误;
B.碳酸氢钠不稳定,受热易分解产生二氧化碳,能使面团松软,可做食品膨松剂,B正确 ;
C.青铜是在纯铜(紫铜)中加入锡或铅的合金,黄铜为是由铜和锌所组成的合金,两者均属于混合物,不是铜单质,C错误;
D.钠元素灼烧显黄色,D错误;
故选B。
8. 一种实现二氧化碳固定及再利用的反应如下:
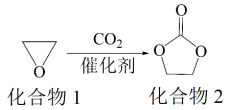
下列叙述正确的是
A. 化合物1分子中的所有原子共平面 B. 化合物1与乙醇互为同系物
C. 化合物2分子中含有羟基和酯基 D. 化合物2可以发生开环聚合反应
【答案】D
【解析】
【详解】A.化合物1分子中还有亚甲基结构,其中心碳原子采用sp3杂化方式,所以所有原子不可能共平面,A错误;
B.结构相似,分子上相差n个CH2的有机物互为同系物,上述化合物1为环氧乙烷,属于醚类,乙醇属于醇类,与乙醇结构不相似,不是同系物,B错误;
C.根据上述化合物2的分子结构可知,分子中含酯基,不含羟基,C错误;
D.化合物2分子可发生开环聚合形成高分子化合物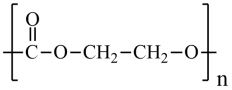 ,D正确;
,D正确;
答案选D。
9. 某白色粉末样品,可能含有![]() 、
、![]() 、
、![]() 和
和![]() 。取少量样品进行如下实验:
。取少量样品进行如下实验:
①溶于水,得到无色透明溶液
②向①的溶液中滴加过量稀盐酸,溶液变浑浊,有刺激性气体逸出。离心分离。
③取②的上层清液,向其中滴加![]() 溶液有沉淀生成。
溶液有沉淀生成。
该样品中确定存在的是
A. ![]() B.
B. ![]() C.
C. ![]() D.
D. ![]()
【答案】A
【解析】
【详解】由题意可知,①取少量样品溶于水得到无色透明溶液,说明固体溶于水且相互之间能共存,②向①的溶液中滴加过量稀盐酸,溶液变浑浊,有刺激性气体放出,说明固体中存在Na2S2O3,发生反应S2O![]() +2H+=S↓+H2O+SO2↑,离心分离,③取②的上层清液,向其中滴加BaCl2溶液,有沉淀生成,则沉淀为BaSO4,说明固体中存在Na2SO4,不能确定是否有Na2SO3和Na2CO3,Na2SO3与过量盐酸反应生成二氧化硫,Na2CO3与过量盐酸反应生成二氧化碳,而这些现象可以被Na2S2O3与过量盐酸反应的现象覆盖掉,综上分析,该样品中确定存在的是:Na2SO4、Na2S2O3,
+2H+=S↓+H2O+SO2↑,离心分离,③取②的上层清液,向其中滴加BaCl2溶液,有沉淀生成,则沉淀为BaSO4,说明固体中存在Na2SO4,不能确定是否有Na2SO3和Na2CO3,Na2SO3与过量盐酸反应生成二氧化硫,Na2CO3与过量盐酸反应生成二氧化碳,而这些现象可以被Na2S2O3与过量盐酸反应的现象覆盖掉,综上分析,该样品中确定存在的是:Na2SO4、Na2S2O3,
答案选A。
10. 由实验操作和现象,可得出相应正确结论的是
实验操作 | 现象 | 结论 | |
A | 向NaBr溶液中滴加过量氯水,再加入淀粉KI溶液 | 先变橙色,后变蓝色 | 氧化性: |
B | 向蔗糖溶液中滴加稀硫酸,水浴加热,加入新制的 | 无砖红色沉淀 | 蔗糖未发生水解 |
C | 石蜡油加强热,将产生的气体通入 | 溶液红棕色变无色 | 气体中含有不饱和烃 |
D | 加热试管中的聚氯乙烯薄膜碎片 | 试管口润湿的蓝色石蕊试纸变红 | 氯乙烯加聚 |
A. A B. B C. C D. D
【答案】C
【解析】
【详解】A.向NaBr溶液中滴加过量氯水,溴离子被氧化为溴单质,但氯水过量,再加入淀粉KI溶液,过量的氯水可以将碘离子氧化为碘单质,无法证明溴单质的氧化性强于碘单质,A错误;
B.向蔗糖溶液中滴加稀硫酸,水浴加热后,应加入氢氧化钠溶液使体系呈碱性,若不加氢氧化钠,未反应的稀硫酸会和新制氢氧化铜反应,则不会产生砖红色沉淀,不能说明蔗糖没有发生水解,B错误;
C.石蜡油加强热,产生的气体能使溴的四氯化碳溶液褪色,说明气体中含有不饱和烃,与溴发生加成反应使溴的四氯化碳溶液褪色,C正确;
D.聚氯乙烯加强热产生能使湿润蓝色湿润试纸变红的气体,说明产生了氯化氢,不能说明氯乙烯加聚是可逆反应,可逆反应是指在同一条件下,既能向正反应方向进行,同时又能向逆反应的方向进行的反应,而氯乙烯加聚和聚氯乙烯加强热分解条件不同,D错误;
答案选C。
11. 化合物![]() 可用于电讯器材、高级玻璃的制造。W、X、Y、Z为短周期元素,原子序数依次增加,且加和为21。
可用于电讯器材、高级玻璃的制造。W、X、Y、Z为短周期元素,原子序数依次增加,且加和为21。![]() 分子的总电子数为奇数常温下为气体。该化合物的热重曲线如图所示,在
分子的总电子数为奇数常温下为气体。该化合物的热重曲线如图所示,在![]() 以下热分解时无刺激性气体逸出。下列叙述正确的是
以下热分解时无刺激性气体逸出。下列叙述正确的是
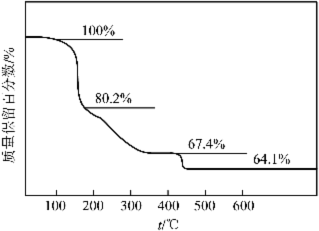
A. W、X、Y、Z的单质常温下均为气体
B. 最高价氧化物的水化物酸性:![]()
C. ![]() 阶段热分解失去4个
阶段热分解失去4个![]()
D. ![]() 热分解后生成固体化合物
热分解后生成固体化合物![]()
【答案】D
【解析】
【分析】化合物(YW4X5Z8·4W2Z)可用于电讯器材、高级玻璃的制造。W、X、Y、Z为短周期元素,原子序数依次增加,且加和为21。该化合物的热重曲线如图所示,在200℃以下热分解时无刺激性气体逸出,则说明失去的是水,即W为H,Z为O,YZ2分子的总电子数为奇数,常温下为气体,则Y为N,原子序数依次增加,且加和为21,则X为B。
【详解】A.X(B)的单质常温下为固体,故A错误;
B.根据非金属性越强,其最高价氧化物的水化物酸性越强,则最高价氧化物的水化物酸性:X(H3BO3)<Y(HNO3),故B错误;
C.根据前面已知200℃以下热分解时无刺激性气体逸出,则说明失去![]() 是水,若100~200℃阶段热分解失去4个H2O,则质量分数
是水,若100~200℃阶段热分解失去4个H2O,则质量分数![]() ,则说明不是失去去4个H2O,故C错误;
,则说明不是失去去4个H2O,故C错误;
D.化合物(NH4B5O8·4H2O)在500℃热分解后若生成固体化合物X2Z3(B2O3),根据硼元素守恒,则得到关系式2NH4B5O8·4H2O~5B2O3,则固体化合物B2O3质量分数为![]() ,说明假设正确,故D正确。
,说明假设正确,故D正确。
综上所述,答案为D。
12. ![]() 电池比能量高,在汽车、航天等领域具有良好的应用前景。近年来科学家研究了一种光照充电
电池比能量高,在汽车、航天等领域具有良好的应用前景。近年来科学家研究了一种光照充电![]() 电池(如图所示)。光照时,光催化电极产生电子
电池(如图所示)。光照时,光催化电极产生电子![]() 和空穴
和空穴![]() ,驱动阴极反应
,驱动阴极反应![]() 和阳极反应(Li2O2+2h+=2Li++O2)对电池进行充电。下列叙述错误的是
和阳极反应(Li2O2+2h+=2Li++O2)对电池进行充电。下列叙述错误的是
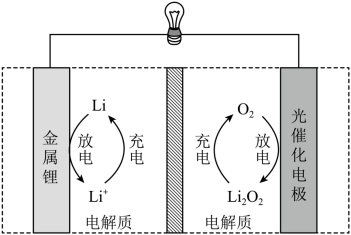
A. 充电时,电池的总反应![]()
B. 充电效率与光照产生的电子和空穴量有关
C. 放电时,Li+从正极穿过离子交换膜向负极迁移
D. 放电时,正极发生反应![]()
【答案】C
【解析】
【分析】充电时光照光催化电极产生电子和空穴,驱动阴极反应(Li++e-=Li+)和阳极反应(Li2O2+2h+=2Li++O2),则充电时总反应为Li2O2=2Li+O2,结合图示,充电时金属Li电极为阴极,光催化电极为阳极;则放电时金属Li电极为负极,光催化电极为正极;据此作答。
【详解】A.光照时,光催化电极产生电子和空穴,驱动阴极反应和阳极反应对电池进行充电,结合阴极反应和阳极反应,充电时电池的总反应为Li2O2=2Li+O2,A正确;
B.充电时,光照光催化电极产生电子和空穴,阴极反应与电子有关,阳极反应与空穴有关,故充电效率与光照产生的电子和空穴量有关,B正确;
C.放电时,金属Li电极为负极,光催化电极为正极,Li+从负极穿过离子交换膜向正极迁移,C错误;
D.放电时总反应为2Li+O2=Li2O2,正极反应为O2+2Li++2e-=Li2O2,D正确;
答案选C。
13. 常温下,一元酸![]() 的
的![]() 。在某体系中,
。在某体系中,![]() 与
与![]() 离子不能穿过隔膜,未电离的
离子不能穿过隔膜,未电离的![]() 可自由穿过该膜(如图所示)。
可自由穿过该膜(如图所示)。
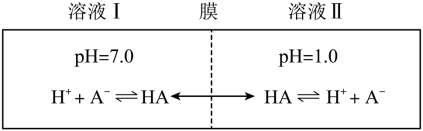
设溶液中![]() ,当达到平衡时,下列叙述正确的是
,当达到平衡时,下列叙述正确的是
A. 溶液Ⅰ中![]()
B. 溶液Ⅱ中的HA的电离度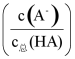 为
为![]()
C. 溶液Ⅰ和Ⅱ中的![]() 不相等
不相等
D. 溶液Ⅰ和Ⅱ中的![]() 之比为
之比为![]()
【答案】B
【解析】
【详解】A.常温下溶液I的pH=7.0,则溶液I中c(H+)=c(OH-)=1×10-7mol/L,c(H+)<c(OH-)+c(A-),A错误;
B.常温下溶液II的pH=1.0,溶液中c(H+)=0.1mol/L,Ka=![]() =1.0×10-3,c总(HA)=c(HA)+c(A-),则
=1.0×10-3,c总(HA)=c(HA)+c(A-),则![]() =1.0×10-3,解得
=1.0×10-3,解得![]() =
=![]() ,B正确;
,B正确;
C.根据题意,未电离的HA可自由穿过隔膜,故溶液I和II中的c(HA)相等,C错误;
D.常温下溶液I的pH=7.0,溶液I中c(H+)=1×10-7mol/L,Ka=![]() =1.0×10-3,c总(HA)=c(HA)+c(A-),
=1.0×10-3,c总(HA)=c(HA)+c(A-),![]() =1.0×10-3,溶液I中c总(HA)=(104+1)c(HA),溶液II的pH=1.0,溶液II中c(H+)=0.1mol/L,Ka=
=1.0×10-3,溶液I中c总(HA)=(104+1)c(HA),溶液II的pH=1.0,溶液II中c(H+)=0.1mol/L,Ka=![]() =1.0×10-3,c总(HA)=c(HA)+c(A-),
=1.0×10-3,c总(HA)=c(HA)+c(A-),![]() =1.0×10-3,溶液II中c总(HA)=1.01c(HA),未电离的HA可自由穿过隔膜,故溶液I和II中的c(HA)相等,溶液I和II中c总(HA)之比为[(104+1)c(HA)]:[1.01c(HA)]=(104+1):1.01≈104,D错误;
=1.0×10-3,溶液II中c总(HA)=1.01c(HA),未电离的HA可自由穿过隔膜,故溶液I和II中的c(HA)相等,溶液I和II中c总(HA)之比为[(104+1)c(HA)]:[1.01c(HA)]=(104+1):1.01≈104,D错误;
答案选B![]()
二、选择题:本题共8小题,每小题6分,共48分。在每小题给出的四个选项中,第14~18题只有一项是符合题目要求的,第19~21题有多项符合题目要求。全部选对的得6分,选对但不全的得3分,有选错的得0分。
14. 2022年3月,中国航天员翟志刚、王亚平、叶光富在离地球表面约![]() 的“天宫二号”空间站上通过天地连线,为同学们上了一堂精彩的科学课。通过直播画面可以看到,在近地圆轨道上飞行的“天宫二号”中,航天员可以自由地漂浮,这表明他们( )
的“天宫二号”空间站上通过天地连线,为同学们上了一堂精彩的科学课。通过直播画面可以看到,在近地圆轨道上飞行的“天宫二号”中,航天员可以自由地漂浮,这表明他们( )
A. 所受地球引力的大小近似为零
B. 所受地球引力与飞船对其作用力两者的合力近似为零
C. 所受地球引力的大小与其随飞船运动所需向心力的大小近似相等
D. 在地球表面上所受引力的大小小于其随飞船运动所需向心力的大小
【答案】C
【解析】
【详解】ABC.航天员在空间站中所受万有引力完全提供做圆周运动的向心力,飞船对其作用力等于零,故C正确,AB错误;
D.根据万有引力公式
![]()
可知在地球表面上所受引力的大小大于在飞船所受的万有引力大小,因此地球表面引力大于其随飞船运动所需向心力的大小,故D错误。
故选C。
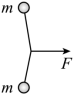
15. 如图,一不可伸长轻绳两端各连接一质量为m的小球,初始时整个系统静置于光滑水平桌面上,两球间的距离等于绳长L。一大小为F的水平恒力作用在轻绳的中点,方向与两球连线垂直。当两球运动至二者相距![]() 时,它们加速度的大小均为( )
时,它们加速度的大小均为( )
A. ![]() B.
B. ![]() C.
C. ![]() D.
D. ![]()
【答案】A
【解析】
【详解】当两球运动至二者相距![]() 时,,如图所示
时,,如图所示
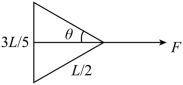
由几何关系可知
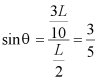
设绳子拉力为![]() ,水平方向有
,水平方向有
![]()
解得
![]()
对任意小球由牛顿第二定律可得
![]()
解得
![]()
故A正确,BCD错误。
故选A。
16. 固定于竖直平面内的光滑大圆环上套有一个小环,小环从大圆环顶端P点由静止开始自由下滑,在下滑过程中,小环的速率正比于( )
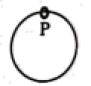
A. 它滑过的弧长
B. 它下降的高度
C. 它到P点的距离
D. 它与P点的连线扫过的面积
【答案】C
【解析】
【详解】如图所示
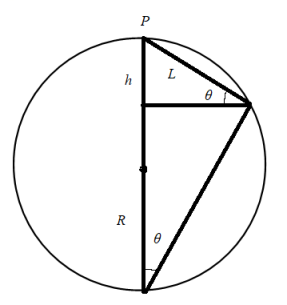
设圆环下降的高度为![]() ,圆环的半径为
,圆环的半径为![]() ,它到P点的距离为
,它到P点的距离为![]() ,根据机械能守恒定律得
,根据机械能守恒定律得
![]()
由几何关系可得
![]()
![]()
联立可得
![]()
可得
![]()
故C正确,ABD错误。
故选C。
17. 一点光源以113W的功率向周围所有方向均匀地辐射波长约为6 × 10 - 7m的光,在离点光源距离为R处每秒垂直通过每平方米的光子数为3 × 1014个。普朗克常量为h = 6.63 × 10 - 34J×s。R约为( )
A. 1 × 102m B. 3 × 102m C. 6 × 102m D. 9 × 102m
【答案】B
【解析】
【详解】一个光子的能量为
E = hν
ν为光的频率,光的波长与频率有以下关系
c = λν
光源每秒发出的光子的个数为
![]()
P为光源的功率,光子以球面波的形式传播,那么以光源为原点的球面上的光子数相同,此时距光源的距离为R处,每秒垂直通过每平方米的光子数为3 × 1014个,那么此处的球面的表面积为
S = 4πR2
则
![]()
联立以上各式解得
R ≈ 3 × 102m
故选B。
18. 安装适当的软件后,利用智能手机中的磁传感器可以测量磁感应强度B。如图,在手机上建立直角坐标系,手机显示屏所在平面为xOy面。某同学在某地对地磁场进行了四次测量,每次测量时y轴指向不同方向而z轴正向保持竖直向上。根据表中测量结果可推知( )
测量序号 | Bx/μT | By/μT | Bz/μT |
1 | 0 | 21 | - 45 |
2 | 0 | - 20 | - 46 |
3 | 21 | 0 | - 45 |
4 | - 21 | 0 | - 45 |
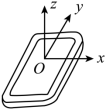
A. 测量地点位于南半球
B. 当地的地磁场大小约为50μT
C![]() 第2次测量时y轴正向指向南方
第2次测量时y轴正向指向南方
D. 第3次测量时y轴正向指向东方
【答案】BC
【解析】
【详解】A.如图所示
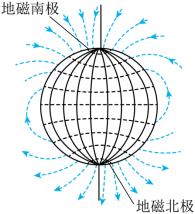
地球可视为一个磁偶极,磁南极大致指向地理北极附近,磁北极大致指向地理南极附近。通过这两个磁极的假想直线(磁轴)与地球的自转轴大约成11.3度的倾斜。由表中z轴数据可看出z轴的磁场竖直向下,则测量地点应位于北半球,A错误;
B.磁感应强度为矢量,故由表格可看出此处的磁感应强度大致为
![]()
计算得
B ≈ 50μT
B正确;
CD.由选项A可知测量地在北半球,而北半球地磁场指向北方斜向下,则第2次测量,测量![]() ,故y轴指向南方,第3次测量
,故y轴指向南方,第3次测量![]() ,故x轴指向北方而y轴则指向西方,C正确、D错误。
,故x轴指向北方而y轴则指向西方,C正确、D错误。
故选BC。
19. 如图,两对等量异号点电荷![]() 、
、![]() 固定于正方形的4个项点上。L、N是该正方形两条对角线与其内切圆的交点,O为内切圆的圆心,M为切点。则( )
固定于正方形的4个项点上。L、N是该正方形两条对角线与其内切圆的交点,O为内切圆的圆心,M为切点。则( )

A. L和N两点处的电场方向相互垂直
B. M点的电场方向平行于该点处的切线,方向向左
C. 将一带正电的点电荷从M点移动到O点,电场力做正功
D. 将一带正电的点电荷从L点移动到N点,电场力做功为零
【答案】AB
【解析】
【详解】A.两个正电荷在N点产生的场强方向由N指向O,N点处于两负电荷连线的中垂线上,则两负电荷在N点产生的场强方向由N指向O,则N点的合场强方向由N指向O,同理可知,两个负电荷在L处产生的场强方向由O指向L,L点处于两正电荷连线的中垂线上,两正电荷在L处产生的场强方向由O指向L,则L处的合场方向由O指向L,由于正方向两对角线垂直平分,则L和N两点处的电场方向相互垂直,故A正确;
B.正方向底边的一对等量异号电荷在M点产生的场强方向向左,而正方形上方的一对等量异号电荷在M点产生的场强方向向右,由于M点离上方一对等量异号电荷距离较远,则M点的场方向向左,故B正确;
C.由图可知,M和O点位于两等量异号电荷的等势线上,即M和O点电势相等,所以将一带正电的点电荷从M点移动到O点,电场力做功为零,故C错误;
D.由图可知,L点的电势低于N点电势,则将一带正电的点电荷从L点移动到N点,电场力做功不为零,故D错误。
故选AB。
20. 质量为![]() 的物块在水平力F的作用下由静止开始在水平地面上做直线运动,F与时间t的关系如图所示。已知物块与地面间的动摩擦因数为0.2,重力加速度大小取
的物块在水平力F的作用下由静止开始在水平地面上做直线运动,F与时间t的关系如图所示。已知物块与地面间的动摩擦因数为0.2,重力加速度大小取![]() 。则( )
。则( )
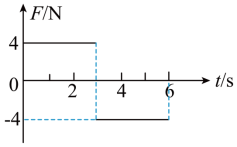
A. ![]() 时物块的动能为零
时物块的动能为零
B. ![]() 时物块回到初始位置
时物块回到初始位置
C. ![]() 时物块的动量为
时物块的动量为![]()
D. ![]() 时间内F对物块所做的功为
时间内F对物块所做的功为![]()
【答案】AD
【解析】
【详解】物块与地面间![]() 摩擦力为
摩擦力为
![]()
AC.对物块从![]() 内由动量定理可知
内由动量定理可知
![]()
即
![]()
得
![]()
3s时物块的动量为
![]()
设3s后经过时间t物块的速度减为0,由动量定理可得
![]()
即
![]()
解得
![]()
所以物块在4s时速度减为0,则此时物块的动能也为0,故A正确,C错误;
B.![]() 物块发生的位移为x1,由动能定理可得
物块发生的位移为x1,由动能定理可得
![]()
即
![]()
得
![]()
![]() 过程中,对物块由动能定理可得
过程中,对物块由动能定理可得
![]()
即
![]()
得
![]()
![]() 物块开始反向运动,物块的加速度大小为
物块开始反向运动,物块的加速度大小为
![]()
发生的位移为
![]()
即6s时物块没有回到初始位置,故B错误;
D.物块在6s时的速度大小为
![]()
![]() 拉力所做的功为
拉力所做的功为
![]()
故D正确。
故选AD。
21. 一种可用于卫星上的带电粒子探测装置,由两个同轴的半圆柱形带电导体极板(半径分别为R和![]() )和探测器组成,其横截面如图(a)所示,点O为圆心。在截面内,极板间各点的电场强度大小与其到O点的距离成反比,方向指向O点。4个带正电的同种粒子从极板间通过,到达探测器。不计重力。粒子1、2做圆周运动,圆的圆心为O、半径分别为
)和探测器组成,其横截面如图(a)所示,点O为圆心。在截面内,极板间各点的电场强度大小与其到O点的距离成反比,方向指向O点。4个带正电的同种粒子从极板间通过,到达探测器。不计重力。粒子1、2做圆周运动,圆的圆心为O、半径分别为![]() 、
、![]() ;粒子3从距O点
;粒子3从距O点![]() 的位置入射并从距O点
的位置入射并从距O点![]() 的位置出射;粒子4从距O点
的位置出射;粒子4从距O点![]() 的位置入射并从距O点
的位置入射并从距O点![]() 的位置出射,轨迹如图(b)中虚线所示。则( )
的位置出射,轨迹如图(b)中虚线所示。则( )

A. 粒子3入射时的动能比它出射时的大
B. 粒子4入射时的动能比它出射时的大
C. 粒子1入射时的动能小于粒子2入射时的动能
D. 粒子1入射时的动能大于粒子3入射时的动能
【答案】BD
【解析】
【详解】C.在截面内,极板间各点的电场强度大小与其到O点的距离成反比,可设为
![]()
带正电的同种粒子1、2在均匀辐向电场中做匀速圆周运动,则有
![]() ,
,![]()
可得
![]()
即粒子1入射时的动能等于粒子2入射时的动能,故C错误;
A.粒子3从距O点![]() 的位置入射并从距O点
的位置入射并从距O点![]() 的位置出射,做向心运动,电场力做正功,则动能增大,粒子3入射时的动能比它出射时的小,故A错误;
的位置出射,做向心运动,电场力做正功,则动能增大,粒子3入射时的动能比它出射时的小,故A错误;
B.粒子4从距O点![]() 的位置入射并从距O点
的位置入射并从距O点![]() 的位置出射,做离心运动,电场力做负功,则动能减小,粒子4入射时的动能比它出射时的大,故B正确;
的位置出射,做离心运动,电场力做负功,则动能减小,粒子4入射时的动能比它出射时的大,故B正确;
D.粒子3做向心运动,有
![]()
可得
![]()
粒子1入射时的动能大于粒子3入射时的动能,故D正确;
故选BD。
三、非选择题:共174分。第22~32题为必考题,每个试题考生都必须作答。第33~38为选考题,考生依据要求作答。
(一)必考题:共129分。
22. 用雷达探测一高速飞行器的位置。从某时刻(![]() )开始的一段时间内,该飞行器可视为沿直线运动,每隔
)开始的一段时间内,该飞行器可视为沿直线运动,每隔![]() 测量一次其位置,坐标为x,结果如下表所示:
测量一次其位置,坐标为x,结果如下表所示:
| 0 | 1 | 2 | 3 | 4 | 5 | 6 |
| 0 | 507 | 1094 | 1759 | 2505 | 3329 | 4233 |
回答下列问题:
(1)根据表中数据可判断该飞行器在这段时间内近似做匀加速运动,判断的理由是:______;
(2)当![]() 时,该飞行器速度的大小
时,该飞行器速度的大小![]() ______
______![]() ;
;
(3)这段时间内该飞行器加速度的大小![]() ______
______![]() (保留2位有效数字)。
(保留2位有效数字)。
【答案】 ①. 相邻1s内的位移之差接近∆x=80m ②. 547 ③. 79
【解析】
【详解】(1)[1]第1s内的位移507m,第2s内的位移587m,第3s内的位移665m,第4s内的位移746m,第5s内的位移824m,第6s内的位移904m,则相邻1s内的位移之差接近∆x=80m,可知判断飞行器在这段时间内做匀加速运动;
(2)[2]当x=507m时飞行器的速度等于0-2s内的平均速度,则
![]()
(3)[3]根据
![]()
23. 一同学探究阻值约为![]() 的待测电阻
的待测电阻![]() 在
在![]() 范围内的伏安特性。可用器材有:电压表V(量程为
范围内的伏安特性。可用器材有:电压表V(量程为![]() ,内阻很大),电流表A(量程为
,内阻很大),电流表A(量程为![]() ,内阻为
,内阻为![]() ),电源E(电动势约为
),电源E(电动势约为![]() ,内阻不计),滑动变阻器R(最大阻值可选
,内阻不计),滑动变阻器R(最大阻值可选![]() 或
或![]() ),定值电阻
),定值电阻![]() (阻值可选
(阻值可选![]() 或
或![]() ),开关S,导线若干。
),开关S,导线若干。
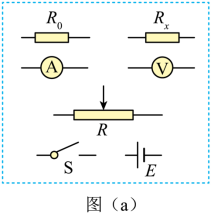
(1)要求通过![]() 的电流可在
的电流可在![]() 范围内连续可调,在答题卡上将图(a)所示的器材符号连线,画出实验电路的原理图________;
范围内连续可调,在答题卡上将图(a)所示的器材符号连线,画出实验电路的原理图________;
(2)实验时,图(a)中的R应选最大阻值为______(填“![]() ”或“
”或“![]() ”)的滑动变阻器,
”)的滑动变阻器,![]() 应选阻值为______(填“
应选阻值为______(填“![]() ”或“
”或“![]() ”)的定值电阻;
”)的定值电阻;
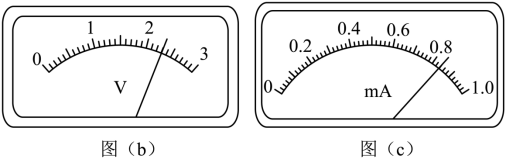
(3)测量多组数据可得![]() 的伏安特性曲线。若在某次测量中,电压表、电流麦的示数分别如图(b)和图(c)所示,则此时
的伏安特性曲线。若在某次测量中,电压表、电流麦的示数分别如图(b)和图(c)所示,则此时![]() 两端的电压为______V,流过
两端的电压为______V,流过![]() 的电流为_____
的电流为_____![]() ,此组数据得到的
,此组数据得到的![]() 的阻值为______
的阻值为______![]() (保留3位有效数字)。
(保留3位有效数字)。
【答案】 ①. 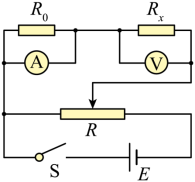 ②.
②. ![]() ③.
③. ![]() ④.
④. ![]() ⑤.
⑤. ![]() ⑥.
⑥. ![]()
【解析】
【详解】(1)[1]电流表内阻已知,电流表与![]() 并联扩大电流表量程,进而准确测量通过
并联扩大电流表量程,进而准确测量通过![]() 的电流,电压表单独测量
的电流,电压表单独测量![]() 的电压;滑动变阻器采用分压式接法,电表从
的电压;滑动变阻器采用分压式接法,电表从![]() 开始测量,满足题中通过
开始测量,满足题中通过![]() 的电流从
的电流从![]() 连续可调,电路图如下
连续可调,电路图如下
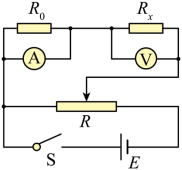
(2)[2]电路中![]() 应选最大阻值为
应选最大阻值为![]() 的滑动变阻器,方便电路的调节,测量效率高、实验误差小;
的滑动变阻器,方便电路的调节,测量效率高、实验误差小;
[3]通过![]()
![]() 电流最大为
电流最大为![]() ,需要将电流表量程扩大为原来的
,需要将电流表量程扩大为原来的![]() 倍,根据并联分流的规律示意图如下
倍,根据并联分流的规律示意图如下
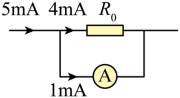
根据并联分流,即并联电路中电流之比等于电阻的反比,可知
![]()
解得
![]()
(3)[4]电压表每小格表示![]() ,向后估读一位,即
,向后估读一位,即![]() ;
;
[5]电流表每小格表示![]() ,本位估读,即
,本位估读,即![]() ,电流表量程扩大
,电流表量程扩大![]() 倍,所以通过
倍,所以通过![]() 的电流为
的电流为![]() ;
;
[6]根据欧姆定律可知
![]()
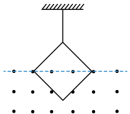
24. 如图,一不可伸长的细绳的上端固定,下端系在边长为![]() 的正方形金属框的一个顶点上。金属框的一条对角线水平,其下方有方向垂直于金属框所在平面的匀强磁场。已知构成金属框的导线单位长度的阻值为
的正方形金属框的一个顶点上。金属框的一条对角线水平,其下方有方向垂直于金属框所在平面的匀强磁场。已知构成金属框的导线单位长度的阻值为![]() ;在
;在![]() 到
到![]() 时间内,磁感应强度大小随时间t的变化关系为
时间内,磁感应强度大小随时间t的变化关系为![]() 。求:
。求:
(1)![]() 时金属框所受安培力的大小;
时金属框所受安培力的大小;
(2)在![]() 到
到![]() 时间内金属框产生的焦耳热。
时间内金属框产生的焦耳热。
【答案】(1)![]() ;(2)0.016J
;(2)0.016J
【解析】
【详解】(1)金属框的总电阻为
![]()
金属框中产生的感应电动势为
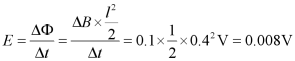
金属框中的电流为
![]()
t=2.0s时磁感应强度![]()
![]()
金属框处于磁场中的有效长度为
![]()
此时金属框所受安培力大小为
![]()
(2)![]() 内金属框产生的焦耳热为
内金属框产生的焦耳热为
![]()
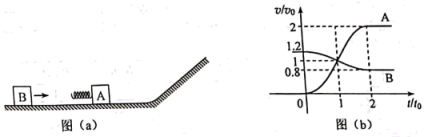
25. 如图(a),一质量为m的物块A与轻质弹簧连接,静止在光滑水平面上:物块B向A运动,![]() 时与弹簧接触,到
时与弹簧接触,到![]() 时与弹簧分离,第一次碰撞结束,A、B的
时与弹簧分离,第一次碰撞结束,A、B的![]() 图像如图(b)所示。已知从
图像如图(b)所示。已知从![]() 到
到![]() 时间内,物块A运动的距离为
时间内,物块A运动的距离为![]() 。A、B分离后,A滑上粗糙斜面,然后滑下,与一直在水平面上运动的B再次碰撞,之后A再次滑上斜面,达到的最高点与前一次相同。斜面倾角为
。A、B分离后,A滑上粗糙斜面,然后滑下,与一直在水平面上运动的B再次碰撞,之后A再次滑上斜面,达到的最高点与前一次相同。斜面倾角为![]() ,与水平面光滑连接。碰撞过程中弹簧始终处于弹性限度内。求
,与水平面光滑连接。碰撞过程中弹簧始终处于弹性限度内。求
(1)第一次碰撞过程中,弹簧弹性势能的最大值;
(2)第一次碰撞过程中,弹簧压缩量的最大值;
(3)物块A与斜面间的动摩擦因数。
【答案】(1)![]() ;(2)
;(2)![]() ;(3)
;(3)![]()
【解析】
【详解】(1)当弹簧被压缩最短时,弹簧弹性势能最大,此时![]() 、
、![]() 速度相等,即
速度相等,即![]() 时刻,根据动量守恒定律
时刻,根据动量守恒定律
![]()
根据能量守恒定律
![]()
联立解得
![]()
![]()
(2)同一时刻弹簧对![]() 、
、![]() 的弹力大小相等,根据牛顿第二定律
的弹力大小相等,根据牛顿第二定律
![]()
可知同一时刻
![]()
则同一时刻![]() 、
、![]() 的的瞬时速度分别为
的的瞬时速度分别为
![]()
![]()
根据位移等速度在时间上的累积可得
![]()
![]()
又
![]()
解得
![]()
第一次碰撞过程中,弹簧压缩量的最大值
![]()
(3)物块A第二次到达斜面的最高点与第一次相同,说明物块A第二次与B分离后速度大小仍为![]() ,方向水平向右,设物块A第一次滑下斜面的速度大小为
,方向水平向右,设物块A第一次滑下斜面的速度大小为![]() ,设向左为正方向,根据动量守恒定律可得
,设向左为正方向,根据动量守恒定律可得
![]()
根据能量守恒定律可得
![]()
联立解得
![]()
设在斜面上滑行的长度为![]() ,上滑过程,根据动能定理可得
,上滑过程,根据动能定理可得
![]()
下滑过程,根据动能定理可得
![]()
联立解得
![]()
26. 废旧铅蓄电池的铅膏中主要含有![]() 、
、![]() 、
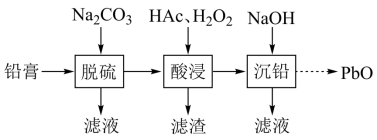
、![]() 和Pb。还有少量Ba、Fe、Al的盐或氧化物等。为了保护环境、充分利用铅资源,通过下图流程实现铅的回收。
和Pb。还有少量Ba、Fe、Al的盐或氧化物等。为了保护环境、充分利用铅资源,通过下图流程实现铅的回收。
一些难溶电解质的溶度积常数如下表:
难溶电解质 |
|
|
|
|
|
|
|
|
|
一定条件下,一些金属氢氧化物沉淀时的![]() 如下表:
如下表:
金属氢氧化物 |
|
|
|
|
开始沉淀的pH | 2.3 | 6.8 | 3.5 | 7.2 |
完全沉淀的pH | 3.2 | 8.3 | 4.6 | 9.1 |
回答下列问题:
(1)在“脱硫”中![]() 转化反应的离子方程式为________,用沉淀溶解平衡原理解释选择
转化反应的离子方程式为________,用沉淀溶解平衡原理解释选择![]() 的原因________。
的原因________。
(2)在“脱硫”中,加入![]() 不能使铅膏中
不能使铅膏中![]() 完全转化,原因是________。
完全转化,原因是________。
(3)在“酸浸”中,除加入醋酸(![]() ),还要加入
),还要加入![]() 。
。
(ⅰ)能被![]() 氧化的离子是________;
氧化的离子是________;
(ⅱ)![]() 促进了金属Pb在醋酸中转化为
促进了金属Pb在醋酸中转化为![]() ,其化学方程式为________;
,其化学方程式为________;
(ⅲ)![]() 也能使
也能使![]() 转化为
转化为![]() ,
,![]() 的作用是________。
的作用是________。
(4)“酸浸”后溶液的pH约为4.9,滤渣的主要成分是________。
(5)“沉铅”的滤液中,金属离子有________。
【答案】(1) ①. PbSO4(s)+CO![]() (aq)= PbCO3(s)+SO
(aq)= PbCO3(s)+SO![]() (aq) ②. 反应PbSO4(s)+CO
(aq) ②. 反应PbSO4(s)+CO![]() (aq)= PbCO3(s)+SO
(aq)= PbCO3(s)+SO![]() (aq)的平衡常数K=
(aq)的平衡常数K=![]() =3.4
=3.4![]() 105>105,PbSO4可以比较彻底的转化为PbCO3
105>105,PbSO4可以比较彻底的转化为PbCO3
(2)反应BaSO4(s)+CO![]() (aq)= BaCO3(s)+SO
(aq)= BaCO3(s)+SO![]() (aq)的平衡常数K=
(aq)的平衡常数K=![]() =0.04<<105,反应正向进行的程度有限
=0.04<<105,反应正向进行的程度有限
(3) ①. Fe2+ ②. Pb+H2O2+2HAc=Pb(Ac)2+2H2O ③. 作还原剂
(4)Fe(OH)3、Al(OH)3
(5)Ba2+、Na+
【解析】
【分析】铅膏中主要含有PbSO4、PbO2、PbO和Pb,还有少量Ba、Fe、Al的盐或氧化物等,向铅膏中加入碳酸钠溶液进行脱硫,硫酸铅转化为碳酸铅,过滤,向所得固体中加入醋酸、过氧化氢进行酸浸,过氧化氢可将溶液中的亚铁离子氧化为铁离子,酸浸后溶液的pH约为4.9,依据金属氢氧化物沉淀时的pH可知,滤渣主要成分为氢氧化铝、氢氧化铁,过滤后,向滤液中加入氢氧化钠溶液进行沉铅,得到氢氧化铅沉淀,滤液中的金属阳离子主要为钠离子和钡离子,氢氧化铅再进行处理得到PbO。
【小问1详解】
“脱硫”中,碳酸钠溶液与硫酸铅反应生成碳酸铅和硫酸钠,反应的离子方程式为:PbSO4(s)+CO![]() (aq)= PbCO3(s)+SO
(aq)= PbCO3(s)+SO![]() (aq),由一些难溶电解质的溶度积常数的数据可知,Ksp(PbCO3)=7.4
(aq),由一些难溶电解质的溶度积常数的数据可知,Ksp(PbCO3)=7.4![]() 10-14,Ksp(PbSO4)=2.5
10-14,Ksp(PbSO4)=2.5![]() 10-8,反应PbSO4(s)+CO
10-8,反应PbSO4(s)+CO![]() (aq)= PbCO3(s)+SO
(aq)= PbCO3(s)+SO![]() (aq)的平衡常数K=
(aq)的平衡常数K=![]() =
=![]() =
=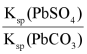 =
=![]() ≈3.4
≈3.4![]() 105>105,说明可以转化的比较彻底,且转化后生成的碳酸铅可由酸浸进入溶液中,减少铅的损失。
105>105,说明可以转化的比较彻底,且转化后生成的碳酸铅可由酸浸进入溶液中,减少铅的损失。
【小问2详解】
反应BaSO4(s)+CO![]() (aq)= BaCO3(s)+SO
(aq)= BaCO3(s)+SO![]() (aq)的平衡常数K=
(aq)的平衡常数K=![]() =
=![]() =
=![]() =
=![]() ≈0.04<<105,说明该反应正向进行的程度有限,因此加入碳酸钠不能使铅膏中的BaSO4完全转化。
≈0.04<<105,说明该反应正向进行的程度有限,因此加入碳酸钠不能使铅膏中的BaSO4完全转化。
【小问3详解】
(i)过氧化氢有氧化性,亚铁离子有还原性,会被过氧化氢氧化为铁离子。
(ii)过氧化氢促进金属Pb在醋酸溶液中转化为Pb(Ac)2,过氧化氢与Pb、HAc发生氧还原反应生成Pb(Ac)2和H2O,依据得失电子守恒和原子守恒可知,反应的化学方程式为:Pb+H2O2+2HAc=Pb(Ac)2+2H2O。
(iii)过氧化氢也能使PbO2转化为Pb(Ac)2,铅元素化合价由+4价降低到了+2价,PbO2是氧化剂,则过氧化氢是还原剂。
【小问4详解】
酸浸后溶液的pH约为4.9,依据金属氢氧化物沉淀时的pH可知,滤渣主要成分为氢氧化铝、氢氧化铁。
【小问5详解】
依据分析可知,加入碳酸钠不能使铅膏中的BaSO4完全转化,铁离子、铝离子转化为了氢氧化铁、氢氧化铝沉淀,铅转化为了氢氧化铅、最终变为了氧化铅,因此沉铅的滤液中,金属离子有Ba2+和加入碳酸钠、氢氧化钠时引入的Na+。
27. 二草酸合铜(Ⅱ)酸钾(![]() )可用于无机合成、功能材料制备。实验室制备二草酸合铜(Ⅱ)酸钾可采用如下步骤:
)可用于无机合成、功能材料制备。实验室制备二草酸合铜(Ⅱ)酸钾可采用如下步骤:
Ⅰ.取已知浓度的![]() 溶液,搅拌下滴加足量
溶液,搅拌下滴加足量![]() 溶液,产生浅蓝色沉淀。加热,沉淀转变成黑色,过滤。
溶液,产生浅蓝色沉淀。加热,沉淀转变成黑色,过滤。
Ⅱ.向草酸(![]() )溶液中加入适量
)溶液中加入适量![]() 固体,制得
固体,制得![]() 和
和![]() 混合溶液。
混合溶液。
Ⅲ.将Ⅱ的混合溶液加热至80-85℃,加入Ⅰ中的黑色沉淀。全部溶解后,趁热过滤。
Ⅳ.将Ⅲ的滤液用蒸汽浴加热浓缩,经一系列操作后,干燥,得到二草酸合铜(Ⅱ)酸钾晶体,进行表征和分析。
回答下列问题:
(1)由![]() 配制Ⅰ中的
配制Ⅰ中的![]() 溶液,下列仪器中不需要的是________(填仪器名称)。
溶液,下列仪器中不需要的是________(填仪器名称)。
(2)长期存放的![]() 中,会出现少量白色固体,原因是________。
中,会出现少量白色固体,原因是________。
(3)Ⅰ中的黑色沉淀是________(写化学式)。
(4)Ⅱ中原料配比为![]() ,写出反应的化学方程式________。
,写出反应的化学方程式________。
(5)Ⅱ中,为防止反应过于剧烈而引起喷溅,加入![]() 应采取________的方法。
应采取________的方法。
(6)Ⅲ中应采用________进行加热![]()
(7)Ⅳ中“一系列操作”包括________。
【答案】(1)分液漏斗和球形冷凝管
(2)![]() 风化失去结晶水生成无水硫酸铜
风化失去结晶水生成无水硫酸铜
(3)CuO (4)3H2C2O4+2K2CO3=2KHC2O4+K2C2O4+2H2O+2CO2↑
(5)分批加入并搅拌 (6)水浴
(7)冷却结晶、过滤、洗涤
【解析】
【分析】取已知浓度的![]() 溶液,搅拌下滴加足量
溶液,搅拌下滴加足量![]() 溶液,产生浅蓝色沉淀氢氧化铜,加热,氢氧化铜分解生成黑色的氧化铜沉淀,过滤,向草酸(
溶液,产生浅蓝色沉淀氢氧化铜,加热,氢氧化铜分解生成黑色的氧化铜沉淀,过滤,向草酸(![]() )溶液中加入适量
)溶液中加入适量![]() 固体,制得
固体,制得![]() 和
和![]() 混合溶液,将
混合溶液,将![]() 和
和![]() 混合溶液加热至80-85℃,加入氧化铜固体,全部溶解后,趁热过滤,将滤液用蒸汽浴加热浓缩、冷却结晶、过滤、洗涤、干燥,得到二草酸合铜(Ⅱ)酸钾晶体。
混合溶液加热至80-85℃,加入氧化铜固体,全部溶解后,趁热过滤,将滤液用蒸汽浴加热浓缩、冷却结晶、过滤、洗涤、干燥,得到二草酸合铜(Ⅱ)酸钾晶体。
【小问1详解】
由![]() 固体配制硫酸铜溶液,需用天平称量一定质量的
固体配制硫酸铜溶液,需用天平称量一定质量的![]() 固体,将称量好的固体放入烧杯中,用量筒量取一定体积的水溶解
固体,将称量好的固体放入烧杯中,用量筒量取一定体积的水溶解![]() ,因此用不到的仪器有分液漏斗和球形冷凝管。
,因此用不到的仪器有分液漏斗和球形冷凝管。
【小问2详解】
![]() 含结晶水,长期放置会风化失去结晶水,生成无水硫酸铜,无水硫酸铜为白色固体。
含结晶水,长期放置会风化失去结晶水,生成无水硫酸铜,无水硫酸铜为白色固体。
【小问3详解】
硫酸铜溶液与氢氧化钠溶液反应生成蓝色的氢氧化铜沉淀,加热,氢氧化铜分解生成黑色的氧化铜沉淀。
【小问4详解】