2010年黑龙江普通高中会考化学真题及答案
可能用到的相对原子质量:H:1 N:14 0:16 Na:23 C1:35.5 Mn:55 Cu:64
第一部分 选择题(全体考生必答,共60分)
一、选择题(本题共30小题,每小题2分,共60分。每小题给出的四个选项中,只有
一项符合题目要求)
1.温室效应、臭氧空洞等全球性环境问题,正在威胁着人类的生存和发展。下列气
体中,能产生温室效应的是
![]()
2.符合砒霜的危险化学品标志是

3.下列气体在通常情况下呈黄绿色的是
A.氯气 B.氢气
C.氨气 D.氮气
4.物质的量的单位是
![]()
5.信息高速公路的骨架是光导纤维,它的主要成分是
![]()
6.下列反应属于吸热反应的是
A.燃烧木炭取暖
B.炸药爆炸
![]()
D.酸与碱的中和反应
7.绘制出第一张元素周期表的科学家是
A.道尔顿 B.阿伏加德罗
C.拉瓦锡 D.门捷列夫
8.在实验室里,应保存在煤油中的药品是
A.氢氧化钠 B.金属钠
C.氧化钠 D.过氧化钠
9.下列元素中不属于主族元素的是
A.磷 B.锂
C.氟 D.氩
10.下列过程,使化学反应速率减慢的是
A.高温炼铁
B.电冰箱存放食物
C.煤块粉碎成煤粉燃烧更充分
D.净化汽车尾气时使用催化剂
11.下列属于离子化合物的是
![]()
12.为检验某![]() 溶液是否变质,可向溶液中加入
溶液是否变质,可向溶液中加入
A.KSCN溶液 B.铁片
C.氯水 D.石蕊试液
13.下列各组离子,能在溶液中大量共存的是
![]()
14.下列各组物质,按化合物、单质、混合物顺序排列的是
A.烧碱、氧气、碘酒 B.生石灰、白磷、熟石灰
C.干冰、铁、氯化氢 D.空气、氮气、胆矾
15.下列试剂中,能用于检验酒精中是否含有水的是
![]()
16.下列反应属于氧化还原反应的是
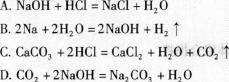
![]()

18.下列混合物,能用分液漏斗进行分离的是
A.水与酒精 B.水与植物油
C.水与醋酸 D.水与蔗糖
19.对于某可逆反应的下列叙述中,不能说明反应一定达到平衡的是
A.正反应速率与逆反应速率相等
B.反应物的浓度与生成物的浓度不再改变
C.在给定条件下反应达到最大限度
D.反应物的浓度与生成物的浓度相等
20.下列分子的空间构型为正四面体的是
A.甲烷 B.苯
C.乙烷 D.乙烯
![]()
A.32 8.67
C.99 D.166
22.绿色化学的核心就是利用化学原理从源头上减少和消除工业生产对环境的污
染,下列属于绿色化学的是
A.废弃塑料的回收和利用 B.污水的治理
c.氢能源代替化石能源 D.“白色污染”物的焚烧


25.当光束通过下列分散系时,能观察到丁达尔效应的是
![]()
26.下列气体中,不能用浓硫酸干燥的是
![]()
27.下列金属中,遇到盐酸或强碱溶液都能放出氢气的是
A.Cu B.Mg
C.Fe D.Al
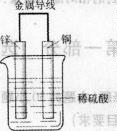 28.关于右图所示装置的叙述正确的是
28.关于右图所示装置的叙述正确的是
A.Zn为负极
B.Zn极发生还原反应
C.Cu为负极
D.Cu极发生氧化反应
29.下列物质中,含有非极性共价键的化合物是
![]()
30.下列反应属于加成反应的是
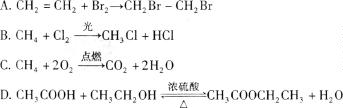
第二部分 非选择题(共40分)
二、必答题(全体考生必答,共20分)
【必修1,2】
31.(2分)小苏打是厨房里的常见物质,是发酵粉的主要成分,请写出小苏打的化学
式 ,若食盐中可能混入了少量小苏打,用下列厨房中的哪
种物质可进行检验 。
A.白酒 B.食醋 C.酱油 D.白糖
32.(5分)下表列出了A—F 6种元素在周期表中的位置
崃 | I A | ⅡA | ⅢA | ⅣA | VA’ | ⅥA | ⅦA |
2 | C | D | |||||
3 | A | B | E | F |
(1)B、C的元素符号分别为 、 ;
(2)D、E两种元素按原子半径由小到大的顺序为 (用元素符号填写);
(3)F元素氢化物的化学式为 ;
(4)A元素的焰色反应呈 色。
33.(4分)有一包白色粉末,其中可能含有
![]() ,现做以下实验。
,现做以下实验。
(1)将部分粉末加入水中,振荡,有白色沉淀生成;
(2)向(1)的悬浊液中加入过量稀硝酸,白色沉淀消失,并有气泡产生;
(3)取少量(2)的溶液滴入![]() 溶液,有白色沉淀生成。
溶液,有白色沉淀生成。
根据上述实验现象,判断白色粉末中一定含有 (填化学式),可能含
自 (填化学式)。写出(3)中有关反应的离子方程式 。
34.(4分)某探究性学习小组通过实验事实的验证与讨论,认识苯的结构。
提出问题:苯分子的结构是碳碳单键和碳碳双键交替的结构吗?
(1)提出假设:

(2)实验验证:
①往苯中滴加酸性高锰酸钾溶液,现象是 。
②经科学测定,苯分子中6个碳原子之间的化学键 (填“相同”或“不
同”)。
(3)结论:苯分子中 碳碳单键和碳碳双键交替的结构(填“存在”或“不
存在”),为了表示苯分子的结构特点,苯分子的结构简式还可表示为
。
![]()

三、选答题(共20分,考生只能选择一个模块的相关试题作答,且必须用28铅笔将
答题卡上对应的识别码涂黑,若出现下列情况则答题无效:识别码均未涂或多涂;所答题
目与涂黑的识别码标记的模块不一致)
【化学与生活】
36.(10分)
根据表中维生素C的有关信息,回答下列问题:
分子式 | C6H806 |
物理特性 | 可口酸味 |
化学特性 | 还原性,易被氧化 |
重要功能 | 抗坏血病 |
主要存在 | 新鲜水果,绿色蔬菜 |
(1)小明同学在超市中购买了以下食品:苹果、西红柿、薯片、牛肉干,上述食品中,富
含维生素C的是 、 ;
(2)维生素C是一种水溶性维生素,溶液显 性(填“酸”或“碱”),生吃新鲜
蔬菜要比熟吃时,维生素C的损失小,因为维生素C在受热时很容易被
(填“氧化”或“还原”);
(3)维生素c可以治疗的疾病是
A.坏血病 B.脑炎 C.骨折 D.肺炎
37.(10分)有四种常见药物①阿司匹林②青霉素③胃舒平④麻黄碱。请回答下列问
题(填序号)。
(1)由于具有兴奋作用,国际奥委会严禁运动员服用的药物是 ;
(2)某同学胃酸过多,应选用的药物是 ,抗酸药是治疗胃酸过多的一类药
物,写出一种抗酸药中和胃酸的化学方程式 ;
(3)从用药安全角度考虑,使用前要进行皮肤敏感性测试的药物是 ;
(4)滥用药物会导致不良后果,如过量服用引起中毒,应立即停药,并静脉注射
NaHC03的是 。
【化学反应原理】
![]()
(1)溶液①的PH 7(填“>”、“<”或“=”),其原理是 (用电离
方程式表示);
(2)溶液②呈 性(填“酸”、“碱”或“中”)。水解反应是吸热反应,升温可
![]()

37.(10分)氢能是当今国际正在探索的新能源之一。
已知:
![]()
Ⅱ:氢氧燃料电池是符合绿色化学理念的新型发电装置。下图为电池示意
图(电极为铂),根据信息回答下列问题:
(1)请写出氢气燃烧的热化学方程式 ;
(2)氢氧燃料电池的能量转化形式主要是 ,在导线中电子流动方向为
(用a,b表示);
(3)负极反应式为 ;
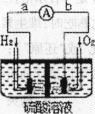 (4)该电池的优点:(答两点即可)
(4)该电池的优点:(答两点即可)
化学答案
一、选择题(本题共30小题,每小题2分,共60分。每小题给出的四个选项中,只有
一项符合题目要求)
题号 | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 |
答案 | B | B | A | A | B | C | D | B | D | B |
题号 | 11 | 12 | 13 | 14 | 15 | 16 | 17 | 18 | 19 | 20 |
答案 | C | A | C | A | B | B | C | B | D | A |
题号 | 21 | 22 | 23 | 24 | 25 | 26 | 27 | 28 | 29 | 30 |
答案 | C | C | A | A | C | D | D | A | C | A |
二、必答题(全体考生必答。共20分)
31.(2分)
![]()
32.(5分)

33.(4分)

34.(4分)
(2)①无明显现象或高锰酸钾溶液不褪色…………………………………(1分)
②相同……………………………………………………………………(1分)
(3)不存在……………………………………………………………………(1分)
![]()
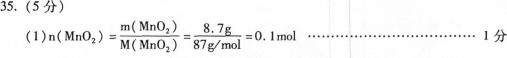

步骤合理即可得分
三、选答题(考生只能选择一个模块的相关试题作答,且必须用28铅笔将答题卡上
对应的识别码涂黑,若出现下列情况则答题无效:识别码均未涂或多涂;所答题目与涂黑
的识别码标记的模块不一致。共20分)
【化学与生活】
36.(10分)
(1)苹果………………………………………………………………………(2分)
西红柿……………………………………………………………………(2分)
(2)酸…………………………………………………………………………(2分)
氧化………………………………………………………………………(2分)
(3)A…………………………………………………………………………(2分)
37.(10分)
(1)④…………………………………………………………………………(2分)
(2)③…………………………………………………………………………(2分)
![]()
(3)②…………………………………………………………………………(2分)
(4)①…………………………………………………………………………(2分)
[化学反应原理]
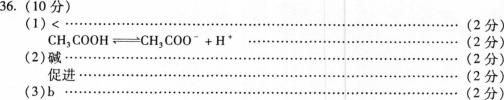

(4)a资源丰富 b可再生 c产物无污染 d能量转化率高
e废弃物较少……………………………………………………………(2分)
(答出其中2项即满分,其它合理答案均给分)
把工作当成自己应该完成的任务,负起自己作为社团的责任。并且在工作的过程中我也学习到了很多我意想不到东西:文章写作,文字处理,工作计划与工作安排、总结等。且做为干事,就是要做好部长分配下来的任务,并敢于主动承担责任。